肺腺癌原因,肺腺癌篩查,肺腺癌預防,肺腺癌治療,肺腺癌藥物
目录
肺腺癌原因、篩查、預防、治療及藥物該如何選擇?這些都是大家關心的重點。肺腺癌原因包括吸菸、空氣污染等,篩查可透過低劑量CT進行。預防需戒菸、保持空氣清新,治療方法有手術、化療等,藥物選擇需根據病情和醫生建議。了解這些資訊,幫助你更好地應對肺腺癌。
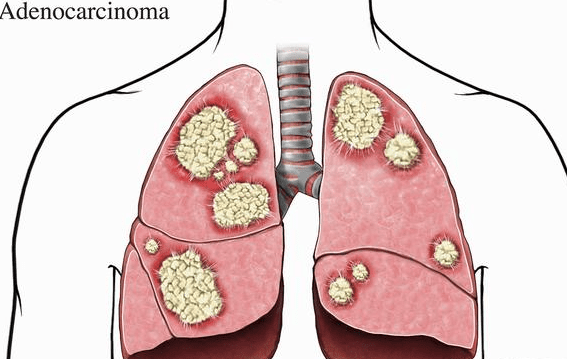
一、肺腺癌原因
1.1 肺腺癌原因:吸煙與二手煙暴露
雖然肺腺癌與吸煙的關聯性相較於鱗狀細胞癌略低,但研究顯示吸煙者罹患肺腺癌的風險仍為非吸煙者的1.5-2倍。香煙煙霧中含有超過60種已知致癌物質,如多環芳香烴、亞硝胺等,可誘導支氣管上皮細胞DNA損傷。值得注意的是,近年來發現低焦油香煙使用者肺腺癌發生率反而上升,可能與吸煙者改變吸煙方式導致致癌物質更深部沉積有關。
1.2 肺腺癌原因:遺傳易感性
全基因組關聯研究(GWAS)已識別出多個肺腺癌遺傳風險位點,包括15q25.1(CHRNA5-CHRNA3基因簇)、5p15.33(TERT基因)等。這些基因多涉及尼古丁代謝、DNA修復及端粒維持等關鍵通路。家族史陽性者患病風險增加1.5-3倍,且發病年齡傾向年輕化。
1.3 肺腺癌原因:環境致癌物暴露
職業性暴露於石棉、砷、鎘、鈹等物質可顯著增加肺腺癌風險。其中石棉暴露者風險增加3-5倍,潛伏期可達20-30年。室內氡氣暴露(特別是高樓層建築)已被確認為獨立風險因素,其衰變產生的α粒子可直接造成肺泡上皮細胞DNA雙鏈斷裂。
二、肺腺癌原因其他相關因素
2.1 大氣污染
PM2.5每增加10μg/m³,肺腺癌風險上升15-20%。細顆粒物可攜帶重金屬及有機致癌物深入肺泡區,誘導慢性炎症反應並產生活性氧簇(ROS),導致上皮-間質轉化(EMT)等癌前病變。
2.2 肺部慢性疾病
特發性肺纖維化患者肺腺癌發生率高達10-15%,可能與異常修復過程中Wnt/β-catenin通路持續活化有關。慢性阻塞性肺病(COPD)患者亦呈現2-3倍風險增加,推測與氧化應激及蛋白酶-抗蛋白酶失衡相關。
2.3 內分泌因素
流行病學數據顯示女性肺腺癌發生率較男性高,且非吸煙女性患者比例顯著。雌激素受體β(ER-β)在肺腺癌組織中過表達,體外實驗證實17β-雌二醇可促進癌細胞增殖,這可能解釋性別差異現象。
2.4 病毒感染
人類乳突病毒(HPV)16/18型DNA在部分肺腺癌組織中被檢出,病毒E6/E7蛋白可能通過抑制p53/Rb通路參與癌變過程。愛潑斯坦-巴爾病毒(EBV)感染與肺淋巴上皮瘤樣癌(特殊亞型腺癌)的關聯性亦有病例報告支持。
三、肺腺癌篩查
3.1 高風險人群定義
根據美國國家肺癌篩查試驗(NLST)標準,推薦55-80歲、30包-年吸煙史且仍在吸煙或戒煙未超過15年者進行年度篩查。亞洲人群研究顯示非吸煙女性亦需納入考量,特別是有家族史或長期廚房油煙暴露者。
3.2 低劑量電腦斷層(LDCT)
相較於胸部X光,LDCT可降低20%肺腺癌死亡率。最新指南建議採用 Lung-RADS 1.1版進行分級管理:4類以上結節應進行PET-CT或組織活检。值得注意的是,約20%篩查發現的毛玻璃樣病變(GGO)可能為浸潤前病變(AAH/AIS),需個體化評估處理時機。
3.3 液體活检技術
循環腫瘤DNA(ctDNA)檢測在早期肺腺癌的敏感性約50-70%,特異性可達95%以上。七種自體抗體檢測(如p53、SOX2抗體)聯合LDCT可提高陽性預測值。表觀遺傳學標記物(如SHOX2、PTGER4甲基化)在痰液中的檢測也展現應用潛力。
四、肺腺癌預防
4.1 一級預防策略
戒煙可使肺腺癌風險隨時間逐步降低,戒煙10年後風險約為持續吸煙者的一半。職業防護需強調工程控制(局部排風)與個人防護裝備(FFP2口罩)的結合。居住環境建議安裝高效微粒空氣(HEPA)過濾系統以降低PM2.5室內濃度。
4.2 化學預防
試驗顯示硒補充劑在低硒人群可能具有保護作用。阿司匹林長期使用者(≥75mg/天,持續5年以上)風險降低10-15%,但需權衡胃腸道出血風險。維生素E補充在吸煙者中反而可能增加風險,凸顯個體化評估的重要性。
4.3 疫苗研發進展
MUC1糖肽疫苗在臨床試驗中展現免疫原性,但三期研究未達預期終點。新興的Neoantigen疫苗針對EGFR/L858R突變的試驗正在進行中。HPV疫苗對於預防HPV相關肺腺癌亞型的潛在價值尚需長期追蹤驗證。
五、肺腺癌治療
5.1 手術治療
早期肺腺癌(I-II期)首選解剖性肺切除(肺葉切除優於亞肺葉切除)加系統性淋巴結清掃。胸腔鏡(VATS)和達文西機器人手術可減少術後疼痛並加速康復。對於多發性GGO,近年提出”根治性亞肺葉切除+術中基因檢測”的新策略。
5.2 放射治療
立體定向體部放射治療(SBRT)對不能手術的早期患者提供5年局部控制率>90%。質子治療在中央型病變中展現劑量學優勢。術後輔助放療的角色仍具爭議,現僅推薦切緣陽性或N2轉移者考慮。
5.3 熱消融技術
經皮射頻消融(RFA)適用於直徑
六、肺腺癌藥物治療
6.1 標靶治療
EGFR-TKIs(如奧希替尼)用於敏感突變患者的中位PFS達18-20個月。ALK抑制劑(如洛拉替尼)對腦轉移控制率尤佳。新興靶點包括RET融合(塞普替尼)、METex14跳躍突變(特泊替尼)等,相關藥物已獲FDA加速批准。
6.2 免疫檢查點抑制劑
PD-1/PD-L1抑制劑單藥用於PD-L1高表達(≥50%)患者的一線治療,ORR約40%。聯合化療方案(如帕博利珠單抗+培美曲塞)顯著延長總生存期。TIGIT抑制劑(如tiragolumab)聯合PD-L1抑制劑的III期研究正在進行中。
6.3 抗血管生成藥物
貝伐珠單抗聯合化療可將ORR提高至50%以上,但需注意出血風險。安羅替尼等小分子TKI在多線治療中展現一定療效。新型雙特異性抗體(如VEGF/ANG2抑制劑)正進行臨床評估。
6.4 抗藥性機制與對策
EGFR-TKI獲得性耐藥中,T790M突變佔50%以上,可選用第三代TKIs克服。旁路激活(如MET擴增)建議聯合抑制策略。組織學轉化(如小細胞轉化)需重新活检指導治療調整。
醫路相伴團隊溫馨提醒:肺腺癌的病因學呈現多因素交互作用的複雜特徵,從基因易感性到環境暴露共同構成發病網絡。精準預防需結合風險分層與個體化干預,而治療策略應基於分子分型動態調整。未來研究方向包括:建立更完善的早期生物標記物體系、開發克服耐藥的創新藥物、優化免疫治療預測模型等,以進一步改善患者預後。
發佈留言