子宮頸癌疫苗,子宮頸癌疫苗接種,子宮頸癌疫苗費用,子宮頸癌疫苗副作用
目录
子宮頸癌疫苗接種重要嗎?疫苗費用、副作用及接種相關資訊,這些都是女性朋友們需要了解的重點。子宮頸癌疫苗能有效預防子宮頸癌,接種費用因疫苗品牌和劑量而異,一般在數千元不等。接種後可能會出現輕微副作用,如注射部位紅腫、發熱等,但通常是暫時性的。了解這些資訊,幫助女性朋友們做出明智的選擇,保護自身健康。
一、子宮頸癌疫苗接種策略
1.1 疫苗作用機制與型別選擇
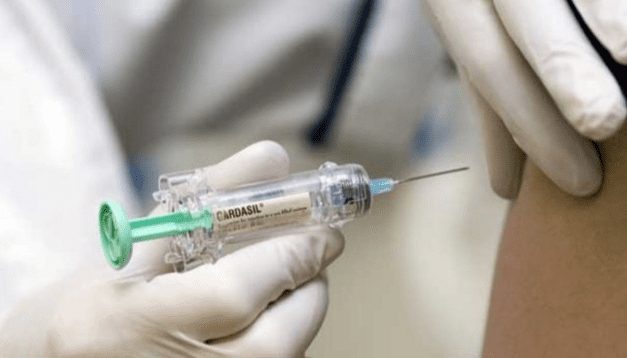
現行核准的HPV疫苗包括二價(Cervarix)、四價(Gardasil 4)及九價(Gardasil 9)三種型號,其核心作用機制為透過病毒樣顆粒(VLPs)誘導產生中和抗體。九價疫苗可預防HPV 16/18/31/33/45/52/58等高風險型別,涵蓋約90%的子宮頸癌致病病毒株。
1.2 目標族群接種時程
世界衛生組織建議主要接種對象為9-14歲女性,採用兩劑接種方案(間隔6個月)。15歲以上女性及免疫功能低下者應接受三劑基礎免疫(0-1-6個月)。男性接種雖無法直接預防子宮頸癌,但可降低HPV傳播及相關口咽癌、肛門癌風險。
1.3 特殊族群接種考量
懷孕婦女建議延後接種,哺乳期非禁忌症。HIV感染者應優先接種九價疫苗,且需完整三劑系列。子宮切除術後女性若術前有HPV暴露史,仍可能受益於疫苗接種。
二、子宮頸癌疫苗費用經濟學分析
2.1 台灣現行疫苗價格結構
依據2023年台灣各醫療院所報價,九價HPV疫苗單劑價格約新台幣5,000-6,500元,完整三劑療程需15,000-19,500元。地方政府公費補貼計劃多限定國中女生族群,自費市場價格受進口關稅及冷鏈成本影響。
2.2 成本效益評估模型
英國衛生經濟學研究顯示,在12歲女性族群實施全面接種,每增加一個品質調整生命年(QALY)的成本約£18,000,符合成本效益閾值。台灣國民健康署評估顯示,公費接種計劃可減少後續抹片檢查及癌前病變治療支出達38%。
2.3 保險給付現況
台灣全民健保尚未涵蓋HPV疫苗常規給付,惟部分企業團險及高端醫療險已將之納入自選項目。新加坡等國採行醫療儲蓄帳戶(Medisave)部分抵免制度,值得參考。
三、子宮頸癌疫苗副作用監測
3.1 常見不良反應分級
第一級反應包括注射部位疼痛(84.3%)、紅斑(25.4%)及腫脹(21.3%),多於48小時內緩解。全身性反應如輕度發燒(10.2%)、頭痛(13.1%)屬自限性。日本厚生勞動省統計顯示嚴重過敏反應發生率約1.7/100萬劑。
3.2 安全性追蹤研究
美國VAERS系統分析2006-2017年間2,800萬劑接種記錄,未發現死亡案例與疫苗具因果關係。丹麥全國世代研究追蹤17萬接種者,顯示疫苗不增加自身免疫疾病風險(HR 0.98, 95%CI 0.90-1.06)。
3.3 風險溝通要點
醫療人員應主動說明注射後暈厥風險(約1/450劑),建議接種後觀察15分鐘。對酵母過敏者禁用四價及九價疫苗。歐洲藥品管理局強調,現有證據不支持疫苗與複雜性局部疼痛症候群(CRPS)的因果關聯。
四、子宮頸癌疫苗疑慮
4.1 生育功能影響爭議
美國兒科學會統合分析顯示,接種組與對照組在受孕時間、流產率及早產率無統計學差異。台灣婦產科醫學會追蹤3,000名接種女性,卵巢儲備功能(AMH值)未受影響。
4.2 替代抹片檢查迷思
疫苗無法提供100%保護,30歲以上女性仍需定期抹片檢查。美國癌症協會建議,即使完成疫苗接種,仍應每5年進行HPV DNA檢測配合抹片檢查。
4.3 效力持久性疑問
瑞典16年追蹤研究顯示,二價疫苗對HPV16/18的保護力維持98%。數學模型預測抗體滴度可持續至少20年,無需追加劑量。免疫記憶研究證實,暴露病毒後抗體水平可快速上升。
4.4 病毒型別替代理論
目前全球監測尚未發現非疫苗型HPV顯著增加。芬蘭研究顯示疫苗型別感染率下降後,非疫苗型感染僅微幅上升4.3%,未達流行病學意義。
五、子宮頸癌疫苗臨床建議
5.1 接種前評估要點
建議進行HPV DNA檢測以排除現行感染,但非接種必要條件。發燒期間應延後接種,輕微感冒不影響疫苗效果。凝血功能異常者可選擇皮下注射。
5.2 混合接種策略
若無法取得相同價數疫苗,ACIP建議後續劑次可轉換為高價數產品。二價與四價疫苗混打研究顯示中和抗體反應良好,但九價疫苗混打數據仍有限。
5.3 追蹤監測計畫
建議建立個人疫苗護照紀錄接種時程。高風險族群接種後6個月可檢測抗體效價,但臨床保護閾值尚未完全確立。異常反應應通報當地藥品不良反應中心。
醫路相伴團隊溫馨提醒:子宮頸癌疫苗展現優異的一級預防效果,全球臨床實證支持其安全性與經濟效益。醫療人員應基於實證醫學提供接種建議,同時持續推動抹片篩檢以達成最佳防癌效果。台灣應考慮擴大公費接種對象,並建立長期本土安全監測資料庫。
發佈留言