胰臟癌存活率,胰臟癌症狀,胰臟癌的診斷,胰臟癌分期,胰臟癌治療方式
胰臟癌存活率如何?胰臟癌的症狀、診斷、分期及治療方式,這些都是患者及家屬關心的重點。胰臟癌早期症狀不明顯,常見有黃疸、腹痛、消瘦等。診斷需結合影像學檢查和腫瘤標誌物檢測。分期根據腫瘤大小、轉移情況分為不同階段。治療方式包括手術切除、化療、放療等,具體選擇需根據患者病情和身體狀況決定。
一、胰臟的位置與生理功能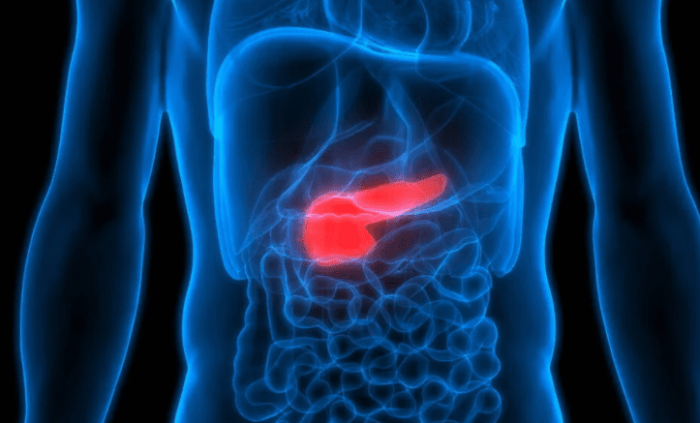
胰臟(Pancreas)位於後腹腔區,橫跨第一至第二腰椎前方,解剖學上可分為頭部、頸部、體部及尾部四部分。其頭部被十二指腸C型彎曲包繞,尾部延伸至脾門處。作為兼具外分泌與內分泌功能的複合性腺體,胰臟每日分泌約1.5-3公升富含消化酶的鹼性胰液,經主胰管(Wirsung duct)排入十二指腸。
外分泌功能主要由腺泡細胞(Acinar cells)負責,分泌胰蛋白酶原、胰脂肪酶等消化酶;內分泌功能則由胰島(Islets of Langerhans)的α、β細胞執行,分別調控昇糖素(Glucagon)與胰島素(Insulin)的分泌。此種特殊的雙重功能特性,使得胰臟病變往往伴隨複雜的代謝異常。
二、胰臟癌的病理學定義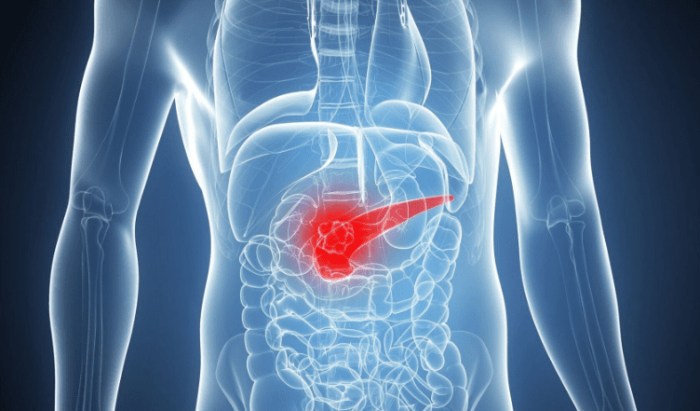
臨床上所謂的胰臟癌(Pancreatic cancer),約90%為胰管腺癌(Pancreatic ductal adenocarcinoma, PDAC),源自胰管上皮細胞的惡性轉化。此類腫瘤具有顯著的間質纖維化特徵(Desmoplastic reaction),且早期即易發生神經周圍浸潤(Perineural invasion)與淋巴血管侵犯。
根據WHO分類,胰臟惡性腫瘤尚包含胰臟神經內分泌腫瘤(PNET)、腺泡細胞癌等罕見類型,其生物學行為與預後均與PDAC有顯著差異。本文主要探討PDAC的相關臨床議題。
三、胰臟癌症狀
早期胰臟癌常無特異性症狀,隨著腫瘤進展可能出現下列典型表現:
1. 上腹部疼痛
約70%患者出現持續性上腹悶痛,疼痛常放射至背部,典型特徵為進食後加重、前傾坐位可緩解,此與腫瘤侵犯腹腔神經叢(Celiac plexus)密切相關。
2. 阻塞性黃疸
胰頭腫瘤壓迫膽總管時,會導致進行性無痛性黃疸,伴隨茶色尿、灰白便及皮膚搔癢。實驗室檢查可見直接型膽紅素升高、鹼性磷酸酶(ALP)顯著上升。
3. 體重減輕與惡病質
約90%患者在診斷時已有明顯體重下降(>10%),其機制包含胰酶分泌不足導致的吸收不良、腫瘤相關代謝亢進及厭食等因素。
4. 新發糖尿病
約15-20%患者在腫瘤診斷前2年內出現血糖控制惡化,可能與β細胞功能受損或腫瘤分泌糖尿病相關因子有關。
5. 其他症狀
包括脂肪瀉(Steatorrhea)、靜脈血栓(Trousseau syndrome)、急性胰臟炎發作等。值得注意的是,約5%患者完全無症狀,係因影像學檢查偶然發現。
四、胰臟癌的高風險族群
流行病學研究確認以下人群具較高罹病風險:
1. 遺傳因素
約10%病例具家族聚集性,與BRCA2、PALB2、CDKN2A等基因突變相關。遺傳性胰臟炎(PRSS1突變)、Peutz-Jeghers症候群患者的終生風險更高達30-40%。
2. 慢性胰臟炎
長期炎症導致腺泡細胞反覆損傷與修復,累積癌變風險較常人高15倍,尤其酒精性胰臟炎更需密切追蹤。
3. 代謝性疾病
第二型糖尿病患者發生胰臟癌的相對風險(RR)為1.5-2.0,若病史超過10年風險進一步升高。肥胖(BMI>30)亦與發病率呈正相關。
4. 環境因素
吸菸者風險較非吸菸者高2-3倍,且呈劑量依賴關係。職業暴露於氯化烴類溶劑亦被認為是潛在危險因子。
五、胰臟癌的診斷與胰臟癌分期
胰臟癌的確診需結合影像學與組織病理證據,標準流程包含:
1. 實驗室檢查
CA19-9是最常用的腫瘤標記,但需注意Lewis抗原陰性者(約10%人口)無法產生CA19-9。肝功能異常(特別是ALP升高)常見於阻塞性黃疸患者。
2. 影像學評估
動態對比增強腹部電腦斷層(CT)是首選工具,可評估腫瘤大小、血管侵犯(如SMV、SMA)及遠處轉移。磁振胰膽管造影(MRCP)對膽胰管系統的顯示尤為清晰。內視鏡超音波(EUS)兼具高解析度與組織取樣優勢,對小於2cm病灶的敏感度達95%。
3. 病理確診
經EUS或CT引導的細針抽吸(FNA)取得細胞學證據,免疫染色檢測CK7、CK19等標記可協助鑑別診斷。液態活檢(Liquid biopsy)檢測循環腫瘤DNA(ctDNA)是新興的無創方法。
4. 分期系統
採用AJCC第8版TNM分期,依據腫瘤局部侵犯程度(T)、淋巴結轉移(N)與遠處轉移(M)進行綜合評定。準確分期對治療策略選擇至關重要。
六、胰臟癌分期與存活率分析
胰臟癌預後與診斷時的分期密切相關,根據SEER資料庫統計:
1. 局部局限性(Stage I-II)
腫瘤局限於胰臟且未侵犯主要血管,約10-15%患者屬此階段。五年存活率可達20-40%,接受根治性手術者胰臟癌存活率約20-28個月。
2. 局部進展期(Stage III)
腫瘤侵犯鄰近血管或臟器但無遠處轉移,佔30-35%病例。傳統上視為不可切除,經新輔助化療後部分患者可能轉化為可手術狀態。胰臟癌存活率約10-12個月。
3. 轉移性疾病(Stage IV)
已出現肝、腹膜等遠處轉移,佔50-55%患者。標準化療下的中位生存期約6-11個月,胰臟癌存活率低於20%。
需特別指出的是,上述數據來自群體統計,個體預後還受體能狀態(Performance status)、分子標記(如dMMR狀態)及治療反應等多因素影響。近年免疫治療與標靶藥物的進展,正逐步改寫特定亞組患者的生存曲線。
七、胰臟癌治療方式
胰臟癌治療需由多專科團隊(MDT)根據分期制定個體化方案:
1. 外科手術
根治性切除是唯一可能治癒的手段,標準術式包含:
- 胰頭腫瘤:胰十二指腸切除術(Whipple procedure)
- 胰體尾腫瘤:遠端胰切除聯合脾臟切除
微創手術(如機器人輔助)在經驗豐富的中心已展現不劣於傳統手術的成效。術前需嚴格評估血管侵犯程度(如SMV/PV是否可重建),R0切除率與預後直接相關。
2. 全身性化療
FOLFIRINOX方案(5-FU+伊立替康+奧沙利鉑)在體能良好患者的中位生存期達11.1個月,優於單用Gemcitabine(6.8個月)。改良版mFOLFIRINOX現常用於輔助治療。Albumin-bound paclitaxel聯合Gemcitabine也是重要選擇。
3. 放射治療
術後輔助放療(45-50.4Gy)對切緣陽性者有益。立體定位放療(SBRT)可精準針對局部病灶,用於不可切除患者的症狀控制。
4. 症狀支持治療
包括膽道支架置入緩解黃疸、腹腔神經叢阻斷術止痛、胰酶補充改善吸收不良等。營養支持與癌症疼痛階梯治療不可或缺。
5. 新興治療
針對BRCA突變患者的PARP抑制劑(如Olaparib)、腫瘤疫苗與CAR-T細胞療法正在臨床試驗階段。分子分型指導的精準醫療是未來研究方向。
醫路相伴團隊溫馨提醒:胰臟癌的低存活率反映其生物學侵襲性與早期診斷困難。臨床醫師應對高風險族群保持警覺,適時運用EUS等工具進行篩檢。治療方面,手術技術的優化與全身治療方案的進步,已使部分患者獲得長期生存機會。未來透過液態活檢提升早期診斷率、開發針對KRAS等驅動基因的標靶藥物,可望進一步改善這「癌王」的治療困境。
發佈留言