肺癌症狀有哪些?篩檢方法與治療存活率全解析
肺癌症狀早期難察覺?專業解析咳嗽、呼吸困難等警訊,並說明肺癌篩檢的重要性與適用對象。提供肺癌飲食營養攝取關鍵指南,深入分析肺癌治療最新技術與療程選擇,同時公開各階段肺癌存活率數據,幫助患者掌握抗癌關鍵資訊,從預防到治療全面守護肺部健康。
目录
各位朋友好,我是專注於肺癌領域的臨床醫師。在診間,我常見到許多病人和家屬帶著恐懼與疑惑前來。肺癌,這個曾經被視為絕症的疾病,隨著醫學進步,已經有了更多對抗的武器。今天,我想以我多年的臨床經驗,用淺顯易懂的方式,帶大家全面認識這個疾病,從警訊、預防、照護到治療選擇,希望能幫助大家更從容地面對挑戰。
1. 肺癌症狀:辨識身體發出的早期警報

肺癌之所以可怕,部分原因在於早期「肺癌症狀」往往非常隱匿,甚至沒有任何不適。許多患者發現時,腫瘤可能已經發展到一定程度,甚至轉移。這就是為什麼我們需要格外留意身體發出的任何非典型訊號。
1.1 呼吸系統相關的肺癌症狀
這是最常見也最容易被聯想到的「肺癌症狀」。如果你出現以下情況,特別是持續超過兩週且無明顯原因(如感冒),務必提高警覺: 持續性咳嗽: 咳嗽是身體的保護機制,但肺癌可能刺激支氣管,導致咳嗽久久不癒,甚至咳嗽性質改變(例如從乾咳變成帶痰或帶血)。 咳血或痰中帶血(咯血): 這是非常值得重視的警訊。不論血量多寡,都應立即就醫檢查。 呼吸困難或喘鳴: 感覺呼吸費力、氣不夠用,或者在呼吸時聽到「咻咻」的喘鳴聲。這可能是腫瘤阻塞氣道或肺部組織受損影響氣體交換所致。 胸痛: 疼痛位置通常在深部、持續性,可能在咳嗽、深呼吸或大笑時加劇。這可能源於腫瘤侵犯胸壁、肋膜或周圍神經。
1.2 全身性與非特異性肺癌症狀
這些症狀容易被忽略或歸咎於其他原因(如工作勞累、年紀大),但它們也可能是「肺癌症狀」的一部分: 原因不明的體重下降: 在沒有刻意節食或增加運動量的情況下,體重明顯減輕(例如幾個月內減輕5%以上)。 持續性疲倦與虛弱: 感覺精力嚴重不足,休息也無法緩解。 食慾不振: 對食物失去興趣。
1.3 肺癌轉移相關症狀
當癌細胞擴散到其他器官,會引發相應位置的症狀,這通常代表肺癌已進展: 骨頭疼痛: 例如背部、髖部疼痛,尤其在夜間加劇。 神經系統症狀: 頭痛、噁心嘔吐、視力模糊、肢體無力或癲癇(轉移至腦部);手臂或臉部麻木刺痛(腫瘤壓迫臂神經叢或頸部交感神經,可能導致霍納氏症候群 – 眼瞼下垂、瞳孔縮小、半邊臉無汗)。 黃疸: 皮膚和眼白變黃(轉移至肝臟)。 頸部或鎖骨上淋巴結腫大。
再次強調,出現上述任一「肺癌症狀」,特別是多重症狀合併或持續存在時,不要猶豫,務必尋求專業醫師的診斷。早期發現的「肺癌症狀」往往是戰勝肺癌的關鍵第一步。
2. 肺癌篩檢:在症狀出現前搶得生機
既然早期的「肺癌症狀」難以察覺,那麼「肺癌篩檢」就扮演了至關重要的角色。我常跟我的病患說:「篩檢不是找麻煩,而是在麻煩找上你之前,先做好準備。」有效的「肺癌篩檢」目標是在肺癌尚未引起症狀、處於最早期(通常是第一期)時就發現它,此時的治癒率最高。
2.1 低劑量電腦斷層掃描
這是目前唯一被大型隨機對照試驗證實,能有效降低高風險族群「肺癌」死亡率的「肺癌篩檢」工具。與傳統X光相比,LDCT能偵測到更小(甚至小於1公分)、更早期的肺部結節(可能是早期肺癌的表現)。它的輻射劑量也比常規CT低得多。
2.2 誰需要接受肺癌篩檢?
並非所有人都需要常規做LDCT篩檢。根據國際指引(如美國預防服務工作組 USPSTF)和台灣本土共識,主要針對「高風險族群」: 年齡介於 50至80歲。 具有 「重度吸菸史」:目前仍在吸菸或過去15年內戒菸,且吸菸史達 「30包-年」(計算方式:每天吸菸包數 x 吸菸年數。例如每天1包吸30年,或每天2包吸15年)。 具有其他肺癌風險因素者(即使吸菸史未達30包-年,但醫師評估風險高):包括直系親屬(父母、兄弟姊妹)有「肺癌」病史、暴露於氡氣、長期職業暴露於石綿、鎘、鉻、鈹、鎳、二氧化矽、煤煙、柴油廢氣等致癌物、曾經罹患其他癌症(特別是頭頸癌、膀胱癌)且接受過胸部放射治療、本身有慢性阻塞性肺病 (COPD) 或肺纖維化病史。
重要提醒: 接受「肺癌篩檢」LDCT前,務必與醫師充分討論利弊。篩檢可能發現需要追蹤但非癌症的結節(偽陽性),帶來不必要的焦慮與後續檢查;也可能出現漏診(偽陰性)。
2.3 篩檢結果的判讀與處理
LDCT篩檢後,影像會根據國際通用的標準(如Lung-RADS)進行分類: 類別1、2: 陰性或良性發現,通常建議一年後再追蹤。 類別3: 可能是良性的結節(通常小於6mm實質結節或特定型態的毛玻璃結節),通常建議6個月後再做一次LDCT追蹤。 類別4A、4B、4X: 可疑惡性結節(較大、有實質成分增長、或具惡性特徵),需要更積極的診斷步驟,例如短期(3個月)追蹤LDCT、PET-CT檢查,或考慮切片診斷(支氣管鏡、電腦斷層導引穿刺等)。 類別S: 發現其他需要關注的問題(如肺氣腫、冠狀動脈鈣化)。
一套完整的「肺癌篩檢」計畫,絕不是做完一次LDCT就結束,後續的追蹤管理計畫同樣重要。我們醫療團隊會根據您的風險程度和檢查結果,制定個人化的追蹤策略。
3. 肺癌飲食:營養是抗癌治療的重要後盾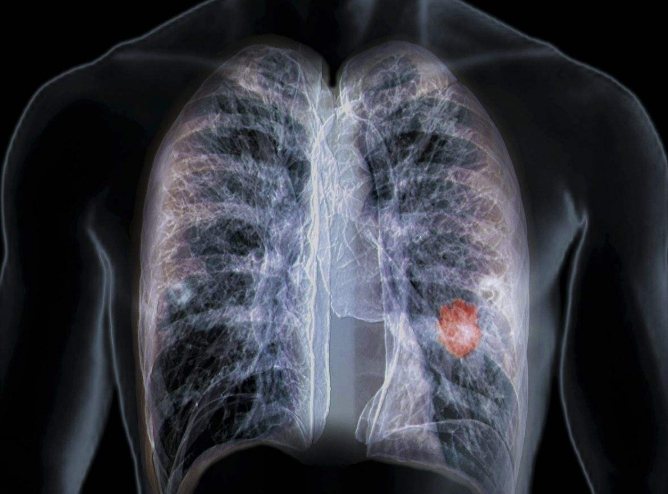
在診間,除了治療計畫,我花很多時間跟病患和家屬談論「肺癌飲食」。為什麼?因為良好的營養狀態,是支撐患者順利完成各種「肺癌治療」(手術、化療、放療、標靶、免疫)、減輕副作用、加速康復、提升生活品質甚至影響「肺癌存活率」的關鍵因素!我看到太多營養不良導致治療中斷或效果打折的案例。
3.1 肺癌飲食的核心目標
「肺癌飲食」並非單指「吃什麼能殺死癌細胞」(目前沒有單一食物能做到),而是圍繞幾個核心目標: 維持體重,避免肌肉流失: 癌症本身和治療都可能導致「惡病質」,即肌肉和脂肪的嚴重消耗。足夠的熱量和蛋白質攝取是根本。 提供足夠蛋白質: 蛋白質是修補組織、維持免疫力、合成抗體對抗感染的重要原料。 補充關鍵微量營養素: 維生素、礦物質協助身體代謝、抗氧化、維持生理機能。 減輕治療副作用: 針對噁心、嘔吐、口乾、口腔潰瘍、味覺改變、腹瀉或便秘等,調整飲食質地和內容。 提升食慾與進食能力。
3.2 肺癌飲食的具體建議
以下是我常給患者的「肺癌飲食」重點: 高熱量高蛋白是首要原則: 優先選擇富含優質蛋白質的食物,例如: 蛋類:蒸蛋、水煮蛋易入口。 豆製品:豆腐、豆干、豆漿(避免脹氣者可少量多次)。 魚類:清蒸魚肉質軟嫩好消化。 雞肉:去皮雞胸肉或雞腿肉。 乳製品:牛奶、起司、無糖優格(若無乳糖不耐)。 必要時可使用商業化高蛋白營養補充品(請諮詢營養師)。 選擇健康的熱量來源: 全穀雜糧類(糙米、燕麥)、適量堅果種子、植物油(橄欖油、苦茶油)。 多樣化蔬果攝取: 提供豐富維生素、礦物質、植化素和膳食纖維。目標是「彩虹飲食」,各種顏色的蔬果都要攝取。但需注意: 治療期間免疫力低,生食蔬果務必清洗乾淨,或考慮煮熟食用。 若有腹瀉,需減少高纖蔬果或去皮去籽;若有便秘,則應增加纖維攝取並搭配足夠水分。 少量多餐: 當胃口不好時,一天吃6小餐比3大餐更容易達成營養目標。隨手準備營養點心(如牛奶麥片、堅果、水果、營養補充品)。 充足水分: 除非有特殊限制(如腎功能異常、心衰竭),每天應攝取足夠水分(約1500-2000ml)。化療時充足水分有助代謝藥物,減輕腎臟負擔。若因副作用導致飲水困難,可嘗試喝水、湯品、果汁、果凍等不同形態補充。 避免有礙健康的食物: 限制油炸、燒烤、加工肉品(香腸、火腿、臘肉)、精緻糖類(甜飲料、蛋糕、糖果)。絕對禁菸酒。
3.3 應對副作用的飲食調整
- 噁心嘔吐: 避免油膩、氣味強烈的食物。選擇清淡、乾燥食物(如蘇打餅乾、土司)。少量多次飲用薑茶或含新鮮檸檬片的水可能有幫忙。飯後勿立即平躺。
- 口腔潰瘍/口乾: 避免酸、辣、太鹹、過熱、粗糙食物。選擇軟質、滑順或流質食物(粥、麵線、蒸蛋、奶昔、湯品)。使用吸管飲用流質。隨身攜帶水壺小口補充水分或漱口保持濕潤。
- 味覺改變: 嘗試不同調味(如檸檬汁、香草、溫和香料)、選擇常溫或稍涼的食物(氣味較不濃烈)、使用非金屬餐具。
- 腹瀉: 避免油炸、高脂、乳製品(若會加重)、高纖蔬果、咖啡因、過甜食物。選擇低渣飲食如白飯、白麵條、蒸蛋、去皮雞肉、嫩葉蔬菜煮熟。補充含鉀食物(香蕉、去油肉湯)和水分。
- 便秘: 增加水分(非常重要!)、適量增加纖維攝取(全穀類、蔬菜水果,但需漸進式以免脹氣)、補充適量油脂(如一小匙橄欖油)、適度活動。
我強烈建議每位肺癌病友,在治療前、中、後期,都應諮詢專業的癌症營養師,制定個人化的「肺癌飲食」計畫,並定期追蹤調整。營養支持絕對是抗癌戰役中不可或缺的一環。
4. 肺癌治療:精準打擊,量身訂作的抗癌策略
「肺癌治療」的發展日新月異,早已不是「一種藥治百人」的時代。作為醫師,我們需要根據肺癌的類型、分期、腫瘤的分子生物學特性(如基因突變)、患者的整體健康狀況等因素,為每位患者量身訂作最佳的治療組合。現在的「肺癌治療」目標不僅是延長生命,更要確保生活品質。
4.1 治療決策的關鍵基石:分期與分類
精準的「肺癌治療」始於精確的分期: 非小細胞肺癌 (NSCLC): 約佔所有肺癌85%,主要包含腺癌、鱗狀細胞癌、大細胞癌。分期採用TNM系統(T:原發腫瘤大小/侵犯範圍;N:局部淋巴結轉移狀況;M:遠端轉移狀況),分為第I、II、III、IV期。 小細胞肺癌 (SCLC): 約佔10-15%,生長快速,早期易轉移。分期較簡化為「局限期」(Limited Stage, LS) 和「擴散期」(Extensive Stage, ES)。
此外,對非小細胞肺癌(特別是肺腺癌)進行「分子檢測」已是指南強烈建議的標準流程。檢測腫瘤組織是否存在特定驅動基因突變,例如: EGFR 突變 ALK 融合基因 ROS1 融合基因 BRAF V600E 突變 KRAS 突變 MET 外顯子14跳躍突變 RET 融合基因 NTRK 融合基因 HER2 突變
這些突變的存在與否,直接決定了是否可使用效果顯著、副作用相對較低的「標靶治療」。免疫治療的選擇也可能與PD-L1的表現量有關。
4.2 多元化的肺癌治療武器庫
依據分期和患者狀況,主要的「肺癌治療」方式包括:
- 手術治療: 適用對象: 早期非小細胞肺癌(第I期、II期及部分III期)且心肺功能可承受手術者。小細胞肺癌極少在早期發現,故手術角色有限。 目標: 完整切除腫瘤及鄰近可能受侵犯的淋巴結,達到根治目的。 術式: 以微創手術為主,如胸腔鏡手術 (VATS) 或機器人輔助手術,傷口小、復原快。切除範圍可能是肺楔形切除、肺節切除或肺葉切除,必要時需全肺切除。
- 放射治療(電療): 適用對象: 早期不適合或不願手術者,可使用立體定位放射治療 (SBRT/SABR) 作為根治性治療。 局部晚期(第III期)非小細胞肺癌,常與化療併用(同步或序貫放化療)。 小細胞肺癌(無論局限期或擴散期)非常重要的一部分。 緩解症狀(如骨轉移疼痛、腦轉移、腫瘤壓迫氣管或上腔靜脈)。 技術: 強度調控放射治療 (IMRT)、影像導航放射治療 (IGRT)、螺旋刀等精準技術,提高腫瘤劑量,減少周圍正常組織傷害。
- 化學治療(化療): 適用對象: 手術後輔助治療:清除可能殘存的癌細胞,降低復發風險(第II期、III期)。 局部晚期(第III期)與放射治療併用。 轉移性(第IV期)肺癌的主要系統性治療之一(尤其無合適標靶可用時)。 小細胞肺癌的基石治療(常與放療併用於局限期;用於擴散期)。 給藥方式: 通常經靜脈注射,多種藥物組合使用。
- 標靶治療: 適用對象: 腫瘤組織經分子檢測帶有特定驅動基因突變的轉移性非小細胞肺癌患者(如EGFR, ALK, ROS1, BRAF等突變者)。這是「肺癌治療」近年最大突破之一。 原理: 藥物如同「導彈」,精準阻斷癌細胞賴以生存和增殖的特定異常分子路徑。 優點: 口服為主,針對性強,副作用通常比傳統化療輕微(但仍有其特定副作用如皮疹、腹瀉、肝功能異常等,需監控)。 挑戰: 腫瘤可能產生抗藥性,需定期追蹤,必要時更換新一代標靶藥物。
- 免疫治療: 適用對象: 轉移性非小細胞肺癌(無論PD-L1表現高低,但高表現者效果更佳)、以及特定條件的小細胞肺癌。也可用於手術切除後的第II-III期非小細胞肺癌的輔助治療(需符合特定條件,如PD-L1高表現)。 原理: 解除癌細胞對免疫系統的「煞車」(如PD-1/PD-L1路徑),重新激活患者自身的免疫T細胞去辨識並攻擊癌細胞。 藥物: 多為靜脈注射。常見藥物如Pembrolizumab, Nivolumab, Atezolizumab, Durvalumab等。 特點: 對於有效者,效果可能非常持久,帶來長期存活希望(所謂的「生存曲線長尾」)。但也可能引發特殊的免疫相關副作用(irAEs),影響任何器官(如皮膚、腸胃、肝、肺、內分泌器官等),需要及早發現並處理。
- 其他治療: 局部治療: 針對寡轉移(轉移處數量很少)或特定症狀緩解,可使用立體定位放射治療 (SBRT)、射頻燒灼術、冷凍治療等。 支持性療法: 貫穿整個治療過程,包括疼痛控制、營養支持、心理社會支持、症狀處理(如喘、咳)、安寧緩和療護等,對於提升生活品質至關重要。
4.3 個人化與多專科團隊合作
現代「肺癌治療」強調「個人化精準醫療」和「多專科團隊合作」(Multidisciplinary Team, MDT)。團隊通常包括胸腔內外科醫師、腫瘤內科醫師、放射腫瘤科醫師、放射科醫師、病理科醫師、核子醫學科醫師、營養師、個案管理師、心理師等。團隊定期討論複雜病例,為患者規劃最適切的治療路徑。例如,一位局部晚期肺癌患者,可能需要先由腫瘤內科給予前導性化療或化放療縮小腫瘤,再由胸腔外科評估手術可行性,術後可能再輔以其他治療。
因此,與您的主治醫師充分溝通,了解各種「肺癌治療」選項的目標(根治性?控制性?緩和性?)、預期效果、可能副作用、對生活的影響以及後續追蹤計畫,是做出明智治療決策的關鍵。
5. 肺癌存活率:理解數字背後的意義與希望
診間裡,「肺癌存活率」是患者和家屬最常詢問,也最難啟齒的問題之一。我理解這個數字的沉重感。作為醫師,我有責任提供基於數據的事實,同時也要傳遞希望,強調「存活率是統計數字,但您是獨一無二的個體」。肺癌的「肺癌存活率」在不同階段差異極大,且隨著治療進步,數字也在不斷改善。
5.1 影響肺癌存活率的關鍵因素
許多因素會影響一個肺癌患者的預後:
- 分期: 這是影響「肺癌存活率」最關鍵的因素。越早期診斷(如第I期),腫瘤局限於肺部,未擴散到淋巴結或遠處器官,治癒機會越高,存活率也越好。一旦發生淋巴結轉移(第II-III期)或遠端轉移(第IV期),存活率顯著下降。這也是為什麼「早期篩檢」發現如此重要。
- 肺癌類型: 非小細胞肺癌 (NSCLC): 整體預後通常優於小細胞肺癌,特別是在早期發現時。 小細胞肺癌 (SCLC): 生長速度快,早期易擴散,整體預後較差。但局限期若能接受積極治療,仍有治癒機會。
- 腫瘤的分子特性與治療選擇: 特別是對於轉移性非小細胞肺癌,如果腫瘤帶有可針對的驅動基因突變(如EGFR, ALK),使用標靶治療後,「肺癌存活率」已大幅提升,許多患者可以存活數年,甚至更久。免疫治療也為許多不帶驅動基因突變的患者帶來長期存活的希望。
- 患者的整體健康狀況: 包括年齡、心肺功能是否良好、有無其他嚴重疾病(如心臟病、糖尿病控制不佳、慢性肺病等)。體能狀態 (Performance Status) 是評估患者能否耐受治療及預後的重要指標。
- 治療反應與副作用管理: 對治療的反應好壞直接影響存活。良好的副作用管理則能讓患者維持體力,順利完成療程,避免中斷。
5.2 理解存活率統計數字
常見的存活率統計指標:
- 五年存活率 (5-Year Survival Rate): 這是最常被引用的指標,指診斷後存活超過五年的患者百分比。它並不代表只能活五年,許多早期患者可以治癒並長期存活。它更像是一個衡量疾病嚴重程度和治療效果的「里程碑」。
- 中位存活期 (Median Survival Time): 指研究中50%患者仍然存活的時間點。例如,若中位存活期為2年,表示有一半患者存活時間超過2年,另一半少於2年。
重要觀念: 統計數字反映的是「過去的」群體平均數據,無法精準預測「個別患者」的存活時間。醫學持續進步,新的藥物和療法不斷問世,現在的「肺癌存活率」通常優於幾年前的數據。
5.3 不同分期與類型的肺癌存活率參考
以下表格提供一個概念性的參考(數據主要參考美國SEER資料庫及大型臨床試驗結果,實際數字因地域、族群、統計年份和最新治療進展而有差異,台灣本土數據趨勢類似):
| 肺癌類型與分期 | 五年相對存活率 (%) (約略參考範圍) | 說明 |
|---|---|---|
| 非小細胞肺癌 (NSCLC) – 局部期 (腫瘤局限於肺部及鄰近淋巴結) | ||
| 第IA期 (T1a/b/c N0 M0) | 80-90% 以上 | 腫瘤小,無淋巴結轉移,手術後治癒率高。 |
| 第IB期 (T2a N0 M0) | 70-80% | 腫瘤稍大但仍無淋巴結轉移。 |
| 第IIA期 (T2b N0 M0; T1a/b/c-T2a N1 M0) | 50-65% | 腫瘤較大或已有同側肺門淋巴結侵犯。 |
| 第IIB期 (T2b N1 M0; T3 N0 M0) | 40-50% | 腫瘤更大或侵犯鄰近結構,或肺門淋巴結轉移。 |
| 局部晚期 (第IIIA-IIIB/C期) | 15-35% | 腫瘤範圍大,侵犯縱膈結構,或/且淋巴結轉移範圍廣(縱膈或對側)。治療積極(如化放療±免疫或手術)可提升機會。 |
| 轉移性 (第IV期) | 約 8-10% (整體) 但分子亞群差異極大 |
無驅動基因且PD-L1低表現:主要靠化療,中位存活期約1年。 具驅動基因 (如EGFR/ALK) 使用標靶:中位存活期可達3-5年或更長,五年存活率顯著提升 (部分研究報告達20-40%以上)。 PD-L1高表現使用免疫:約15-30%患者有長期存活機會。 |
| 小細胞肺癌 (SCLC) | ||
| 局限期 (Limited Stage, LS) | 25-30% (5年) | 腫瘤局限於單側胸腔,可涵蓋於一個可耐受的放射治療範圍。積極同步化放療是標準治療,部分極早期可考慮手術+化療。 |
| 擴散期 (Extensive Stage, ES) | 約 2-5% (5年) 中位存活期:免疫+化療前約8-10個月;加入免疫療法後提升至12-14個月或更長。 |
腫瘤已擴散至對側肺、遠處淋巴結、或遠端器官。治療以化療+免疫為主。少數對治療反應極佳者可能存活較久。 |
解讀「肺癌存活率」數字時,請務必與您的主治醫師深入討論。醫師會根據您的具體情況(分期、類型、分子特性、體能狀態、選擇的治療方案)提供更貼近您個人的預後評估。數字是冰冷的,但醫學的進步和每位患者奮鬥的故事,持續帶來溫暖的希望。
Q&A:解答您對肺癌的常見疑惑
Q1:什麼是肺癌?
A1: 肺癌,顧名思義,是指起源於肺部支氣管或肺泡細胞的惡性腫瘤。這些細胞因為基因突變而失控,異常增生,形成腫塊(腫瘤)。這些癌細胞可能破壞周圍正常肺組織,並有能力透過淋巴系統或血液擴散(轉移)到身體其他部位,如淋巴結、腦部、骨骼、肝臟、腎上腺等。肺癌是台灣乃至全球癌症死亡的主要原因之一。
Q2:肺腺癌有幾期?
A2: 肺腺癌屬於非小細胞肺癌的一種(也是最常見的亞型)。它的分期與其他非小細胞肺癌相同,採用國際通用的TNM分期系統,分為第I期、第II期、第III期和第IV期: 第I期: 腫瘤局限於肺部,未侵犯主要支氣管,無淋巴結轉移(T1-T2a N0 M0)。 第II期: 腫瘤較大或位置較中央(T2b-T3 N0 M0),或腫瘤較小但已有同側肺門附近淋巴結轉移(N1)(T1-T2 N1 M0)。 第III期: 腫瘤侵犯鄰近重要結構(如同側縱膈、心臟、大血管),或/且淋巴結轉移範圍更廣(縱膈或鎖骨上淋巴結)(任何T N2-N3 M0, 或 T3-T4 N1 M0)。這期範圍較廣,細分為IIIA, IIIB, IIIC期,治療複雜度最高。 第IV期: 癌症已發生遠處器官轉移(M1),如對側肺葉、腦、骨、肝、腎上腺等(任何T,任何N,M1)。
Q3:如何確診肺癌?
A3: 確診肺癌需要取得病變組織進行病理學檢查,確認有癌細胞存在。常見的確診方式包括: 1. 影像學檢查發現異常: 通常是起點(如胸部X光發現陰影,或低劑量電腦斷層LDCT篩檢發現結節)。 2. 進一步詳細影像評估: 通常需要做「診斷性」胸部電腦斷層(含顯影劑),評估腫瘤大小、位置、與鄰近結構關係、淋巴結腫大狀況。必要時可能安排全身正子攝影(PET-CT)檢查有無遠處轉移,或腦部MRI檢查。 3. 取得組織切片: 這是確診的「黃金標準」。方法依腫瘤位置和大小而定: 支氣管鏡檢查: 適用於靠近中央氣道的腫瘤。醫師將細長管子(支氣管鏡)經口鼻進入氣管和支氣管,可直視腫瘤並切片或刷檢。 電腦斷層導引穿刺: 適用於周邊型腫瘤。在CT影像導引下,從體表將細針穿過胸壁,到達肺部病灶取得組織。 縱膈腔鏡或內視鏡超音波引導切片 (EBUS/EUS): 用於評估和取得縱膈腫大淋巴結的組織,對分期非常重要。 胸腔鏡手術: 微創手術方式,可直接觀察胸腔內部並取得足夠組織,診斷兼顧治療評估。 胸水分析: 若患者有肋膜積水(胸水),抽出積液檢查是否有癌細胞。 4. 病理診斷與分子檢測: 取得的組織由病理科醫師在顯微鏡下判斷是否為肺癌,並區分類型(腺癌、鱗癌、小細胞癌等)。對於非小細胞肺癌(尤其腺癌),會進一步進行「分子檢測」,尋找是否有可治療的驅動基因突變(如EGFR, ALK等)。
Q4:小細胞肺癌有幾期?
A4: 小細胞肺癌的分期系統較為簡化,主要分為兩大類: 1. 局限期 (Limited Stage, LS): 指腫瘤範圍相對局限,可以被包含在一個「可耐受的放射治療照射範圍」內。通常是指腫瘤僅位於單側胸腔,且淋巴受累範圍未擴散到對側縱膈或鎖骨上淋巴結。相當於TNM分期的第I-IIIB期(但需滿足可單一放射治療野涵蓋)。此期約佔小細胞肺癌診斷時的30%。 2. 擴散期 (Extensive Stage, ES): 指腫瘤範圍已超過局限期定義,例如腫瘤已擴散到對側肺葉、出現惡性肋膜積水或心包膜積水,或已發生遠處器官轉移(如骨、肝、腦、腎上腺等)。相當於TNM分期的第IV期或部分無法單一放射治療野涵蓋的III期。此期約佔70%。這種分期方式主要與治療策略的選擇(如放射治療的角色)和預後密切相關。
關於作者:我是陳醫師,「癌症科學說」的主筆,臺灣大學醫學院研究生學歷。這個部落格要用台灣人最熟悉的方式聊抗癌新知——從夜市炭烤的致癌風險到科技新貴的過勞警訊,我都會用「雞排妹得HPV」這種真實案例來解說。每週固定分享最新標靶藥物解析、抗癌飲食懶人包,還有台灣特有的癌症地圖分析。記住我們的抗癌金句:「早期發現像撿到槍,晚期發現也有盾牌可扛!」
發佈留言